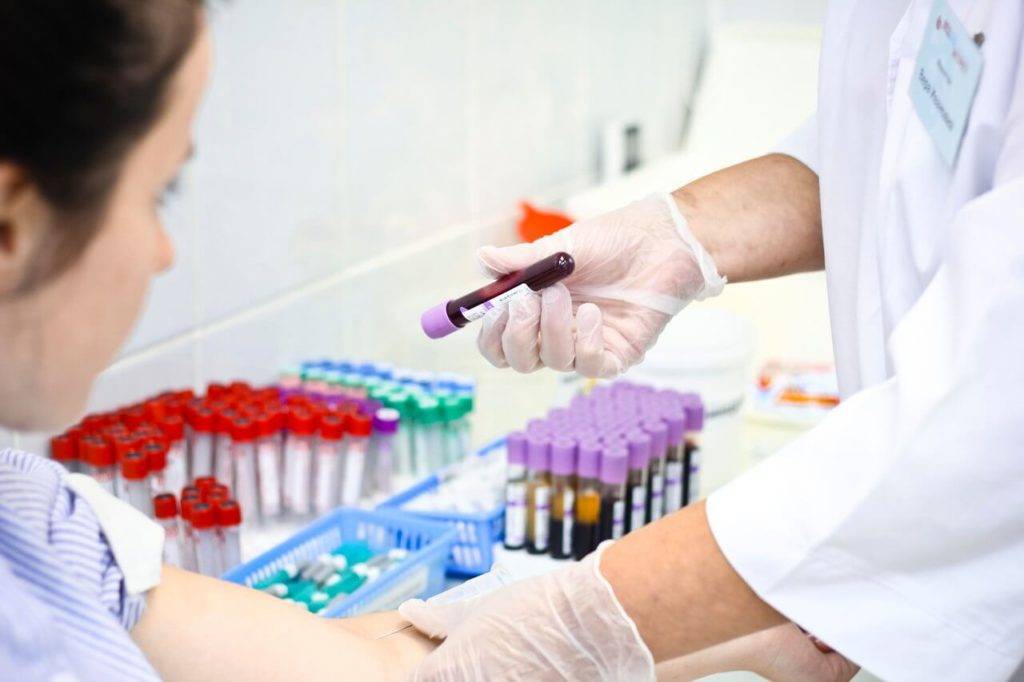
Задержка полового развития описание, причины
Начало полового созревания (пубертатного периода) наступает, когда железы гипоталамуса начинают выделять гонадотропин-рилизинг-гормон. Это вещество является «сигналом» к тому, чтобы организм подростка начинал развивать репродуктивную функцию. Гипофиз отвечает на этот сигнал, выделяя гормоны гонадотропины, стимулирующие рост половых желез — яичек у мужчин и яичников у женщин. Растущие половые железы выделяют тестостерон и эстроген. Эти гормоны, в свою очередь, вызывают развитие вторичных половых признаков, таких как рост волос на лице и набор мышечной массы у мальчиков, развитие груди у девочек, и рост волос на лобке и в подмышечных впадинах, а также первые признаки либидо у представителей обоих полов.
У некоторых подростков половое созревание задерживается и не начинается в положенном для этого периода возрасте.
Конституциональная задержка полового развития — семейная черта, и передается по наследству. Например, если у матери девочки-подростка половое созревание началось не в 14, а в 16 лет, существует высокая вероятность того, что у её дочери половое созревание начнется в аналогичный период. Таким же образом происходит конституциональная задержка пубертатного периода у мальчиков, в особенности, если у отца имелись аналогичные признаки.
При конституциональной задержке полового созревания подростки нормально растут, состояние их здоровья полностью соответствует норме.
Задержать половое созревание могут такие заболевания, как сахарный диабет, воспалительные заболевания кишечника, заболевания почек, муковисцидоз, анемия. Кроме того, дети, проходящие химиотерапию или лучевую терапию, с опозданием вступают в пубертатный период.
Дополнительные причины задержки:
- аутоиммунные заболевания (например, тиреоидит Хашимото, болезнь Аддисона или недостаточность коры надпочечников);
- нарушения функции яичников;
- опухоли гипофиза или гипоталамуса;
- травмы яичек;
- инфекционные заболевания (например, эпидемический паротит);
- скручивание яичка;
- чрезмерное похудение и анорексия у девочек;
- недостаточность веса;
- хромосомные аномалии, в частности, синдром Тернера у девочек и синдром Клайнфельтера у мальчиков.
Синдром Тернера — это заболевание, при котором одна из Х-хромосом у женщин имеет структуру, отклоненную от нормальной, или же одна из Х-хромосом отсутствует полностью. Женщины, рожденные с синдромом Тернера, как правило, бесплодны и нередко имеют другие отклонения в состоянии здоровья. Мужчины с синдромом Клайнфельтера рождаются с дополнительной Х-хромосомой (сочетание хромосом XXY вместо XY);
— синдром Каллмана (свойственен и женщинам, и мужчинам). В ходе этого заболевания нарушается выработка гонадотропина, другие гормоны вырабатываются нормально.
Еще одна немаловажная причина задержки полового созревания — это недостаточность питания, отсутствие необходимых витаминов. Сверстники ребенка, постоянно недополучающего питательных веществ, развиваются раньше и растут активнее. Организм девочки нуждается в некотором количестве подкожного жира для нормального «запуска» процесса менструации и функции яичников. Если жировая прослойка становится слишком тонкой, и девочка намеренно недоедает, можно предположить появление аменореи — отсутствия менструаций.
Излишняя спортивная активность, изматывающие тренировки наряду с сильным стрессом — еще один дополнительный фактор, влияющий на задержку половой зрелости. Интенсивные физические нагрузки, например, танцы, фигурное катание, гимнастика, силовые тренировки и тренировки на выносливость увеличивают вероятность более позднего наступления созревания.
Диагностика задержки пубертатного периода
Диагностика включает в себя следующие методы:
Анализ крови, который необходим для:
- проверки хромосомных нарушений
- измерения уровня гормонов
- проверить наличие сахарного диабета
- проверить наличие заболеваний, провоцирующих нарушение
Рентгенологическое исследование:
- Необходимо для определения зрелости внутренних органов, а также костной ткани.
- Лечение пубертатного периода у детей
Лечение в первую очередь зависит от выяснения причины, спровоцировавшей задержку пубертатного периода. Иногда, для того, чтобы исправить анатомические отклонения больного или при выявлении опухолей, применяется хирургическое лечение. Но, как правило, специальное лечение не нужно. В особых случаях может быть назначена гормональная терапия, чтобы стимулировать выработку гормонов. Иногда в лечении применяется психотерапия для нормализации психического состояния больного, поскольку ребенок чувствует себя неполноценным, в сравнении со своими сверстниками.
При гормональной терапии у девочек, если все рекомендации лечащего врача соблюдены, прогноз благоприятный. Если же лечение отсутствует, или не соблюдаются предписания лечащего врача при приеме гормональных препаратов, возможны следующие последствия:
- Женские половые признаки недоразвиты
- Из половых путей могут наблюдаться кровотечения
- Возможен рак яичников или молочной железы
Что означает гормональное созревание у мальчиков
Гормональное созревание у мальчиков, или становление половой функции, проходит этапы новорожденности, допубертатный, подростковый (пубертат) и зрелости.
Новорожденность
Под влиянием тестостерона еще в период внутриутробного развития формируется пенис и мошонка, затем в нее опускаются яички. Не считается отклонением, если последний процесс завершится уже после рождения – к концу первого года.
Допубертатный период
Следующий период – допубертатный, или до начала гормональных изменений у подростков. В это время тело начинает приобретать мужские черты, а явные изменения видны уже к 13-15 годам:
- развитие плечевого пояса, грудной клетки;
- узкие бедра;
- формирование мускулатуры;
- потемнение кожи мошонки и ее складчатость;
- постепенное увеличение яичек и предстательной железы.
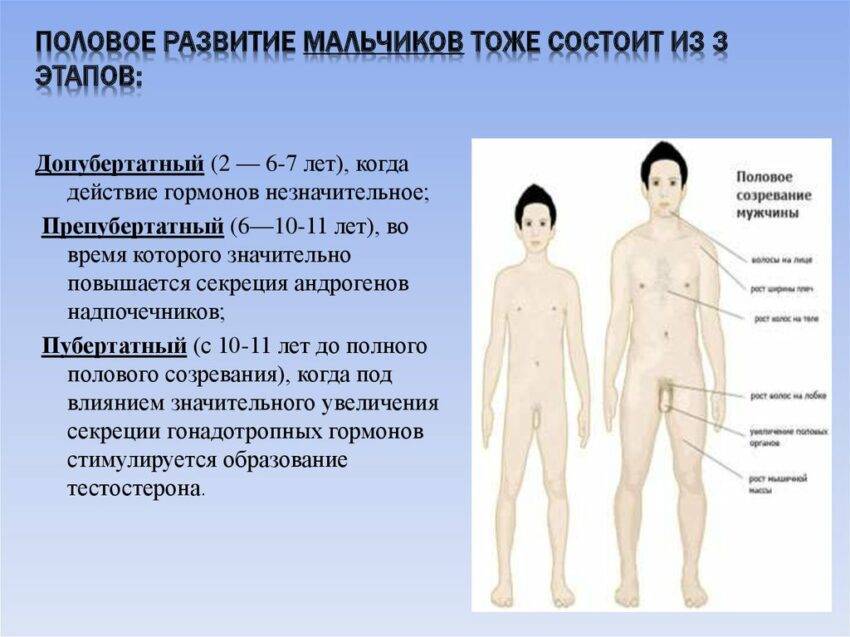
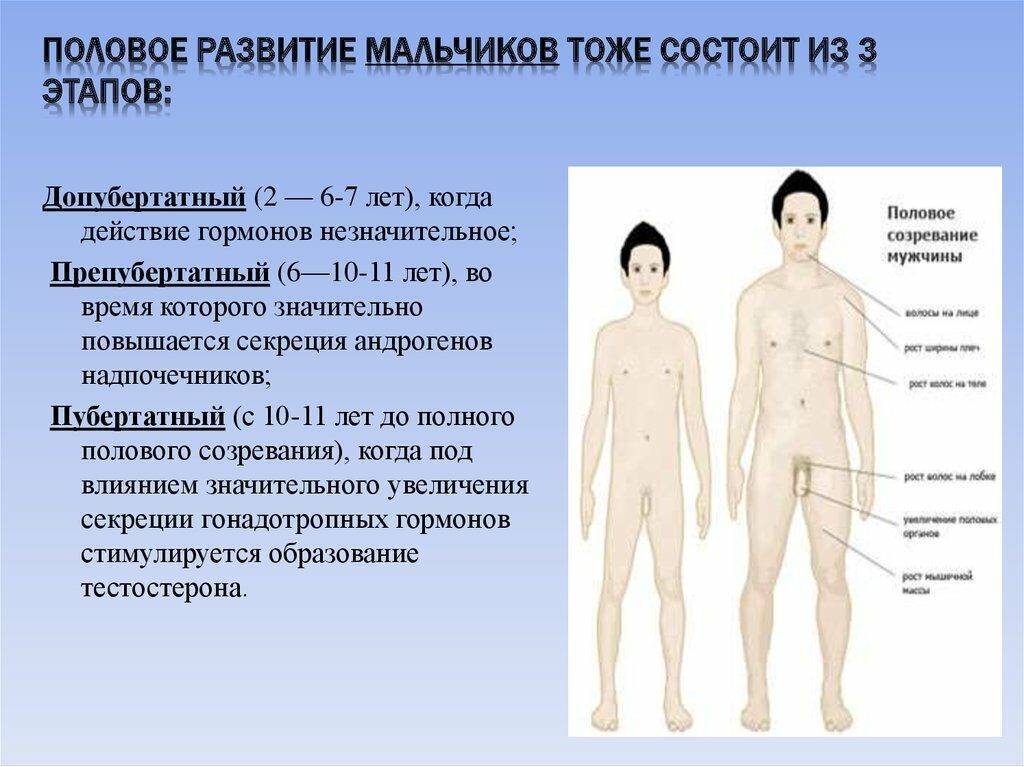
Начало полового созревания, или подростковый этап
Началом полового созревания у мальчиков, которое сопровождается буйством гормонов, считают возрастание объема яичек до 4 см3 (11-12 лет). Через год в утренней моче можно обнаружить сперматозоиды. После яичек растет пенис, возникают эрекции, а затем и выделения спермы ночью – поллюции (с 13,5 до 15 лет). Сперматозоиды становятся более подвижными, а к 14-15 годам приобретают способность оплодотворять яйцеклетку. Сами яички могут увеличиваться до 18-23 лет.
Волосы начинают расти у основания полового члена, затем на лобке в виде треугольника, переходят на бедра и низ живота, по средней линии к пупку (с 12 до 16 лет).
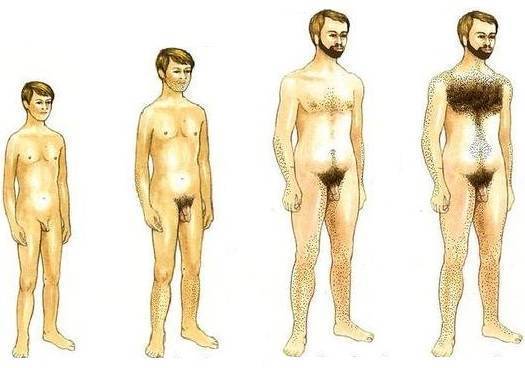 Этапы полового созревания
Этапы полового созревания
Через 0,5-1,5 года оволосение затрагивает подмышки, лицо (усы, борода), околососковую область. Тонкие пушковые волосы грубеют на ногах, руках, спине и груди. Все эти изменения могут иметь варианты, связанные с наследственностью, расовой принадлежностью. Тестостерон влияет на голос – его тембр снижается, а вслед за этим обычно начинается ускоренный рост тела.
Диагностика
Диагностика заболевания предусматривает: измерение роста и веса, вычисление соотношения размеров частей тела, наличие стигм дисморфогенеза, отметка сексуального развития по Таннеру, умственных способностей, подавление аносмии, осмотр врача офтальмолога.
Делается общий анализ мочи, общий и биохимический анализ крови, обязательно проводится полное гормональное обследование. Следует выполнить рентген кисти и запястья для определения скелетного возраста. Девочкам назначается УЗИ органов малого таза, а мальчикам — брюшной полости и яичек.
Гормональная терапия активизирует развитие половых признаков, темпы роста, стимулирует насыщение солями костей, акселерацию гонадотропной системы. Главные критерии назначения гормонов: психические проблемы, склонность к депрессии, проблемы адаптации у мальчиков и девочек.
Главное, в таком медикаментозном лечении — оно не должно вызывать ускорение роста костей. При наследственной задержке полового созревания выбираются внутримышечные инъекции препаратов по 30 мг. Периодичность — один раз в 3 недели на протяжении полугода.
Лекарства группы гонадотропина нежелательно применять для стимулирования полового созревания, т. к. вызывают торможение анатомического роста ребенка. В такой ситуации используют анаболические препараты, имеющие небольшую андрогенную активность. Они не влияют на чрезмерное ускорение скелетного созревания.
У мальчиков
Значительной части мальчиков с задержкой полового развития медикаментозная помощь не требуется, но для них очень важна информационная и психологическая консультация. В более сложной степени заболевания детям предлагают провести тестостероновую терапию в виде инъекции в дозе 40-90 мг в течение 3-6 месяцев (внутримышечно 1 раз в месяц). Другой способ лечения (например, когда требуется повлиять на увеличение объема яичек у мальчиков) — применение тестостерона ундеканоата в течение того же срока (10-30 мг/день).
Более редко применяется подкожная имплантация тестостерона. Но какой бы метод лечения ни был выбран, его необходимо проводить от полугода до года. Из-за видимых внешних анатомических недостатков, у мальчиков всегда наблюдается психически-травмирующее расстройство. У мальчиков часто выявляется гипоплазия яичек, они через время не удлиняются, а остаются шарообразными.
Очень хорошо визуально наблюдается патология развития внешних половых органов: длина пениса менее 6 см, а объем яичек менее 5 квадратных сантиметров, отсутствует отвисание мошонки, волосяной покров незначительный, нет ночных поллюций.
У девочек
Задержка полового развития у девочек наблюдается реже, чем у мальчиков, и медикаментозные методы лечения применяются значительно меньше. Развитие женских половых органов у девочек обычно в 10-12 лет и протекает без патологий. При наличии патологии, лечение имеет смысл назначать не ранее биологического возраста 12 лет (лучше после 13 лет) или возраста костного скелета 10—11 лет.
Препараты нужно применять в небольших дозах, что не допустит чрезмерного ускорения костного развития и непропорционального развития молочных желез, что впоследствии может причинять серьезный дискомфорт для девочки.
Недостаточное развитие женских половых органов лечится известным препаратом этинилэстрадиол, обычно его принимают по 0,02—0,9 мкг/кг в день. В других случаях развитию женских половых органов способствуют конъюгированные эстрогены, они принимаются по 0,2 мг в течении полугода, потом дозу увеличивают. Другим методом лечения задержки пубертата, не менее эффективным, считаются подкожные введения эстрадиола.
Препарат обычно вводится в область ягодиц или бедер примерно через каждые три дня. Важным преимуществом данного метода является возможность его дробления на меньшие дозы, следует учитывать, что большое значение имеет индивидуальная особенность всасывания эстрадиола, вызывающего потребность к постоянному измерению количества эстрогенов в составе крови во время лечения. И по результатам этих измерений, врач изменяет количество лечебного вещества.
Формы заболевания
У болезни есть несколько форм, что позволяет облегчить ее классификацию, предлагаем ознакомиться с распространенными разновидностями состояния:
Конституциональная задержка | Имеет широкое распространение и диагностируется у 60-80% больных. Состояние носит наследственный характер, поскольку при сборе информации удается обнаружить аналогичные проблемы у одного или обоих родителей. |
Соматогенная задержка | Обусловлена иными факторами, ее связывают с нарушениями в процессе питания. Если у подростка есть признаки анорексии, других проблем с пищевым поведением, связанных с недостатком питательных веществ, то может возникнуть задержка пубертата. Состояние также развивается на фоне ожирения, тяжелых патологий в работе печени и органов ЖКТ. |
Ложная генитальная дистрофия | Выступает как форма заболевания, которую часто диагностируют у детей с поражением ЦНС. Подобный диагноз может быть поставлен пациенту любого возраста, но чаще он наблюдается у детей первых трех лет жизни. Причиной возникновения проблемы считают неблагоприятные факторы: инфекционные заболевания (нейроинфекции) и травматические повреждения черепа. |
Функциональная задержка | Связана с повышением уровня пролактина в крови, нередко развивается при опухолях гипофиза или гипоталамуса. В некоторых случаях считается следствием приема определенных медикаментозных препаратов. |
Причины и признаки

Повреждение репродуктивной системы может происходить на трех уровнях, в связи с чем выделяют три формы:
- Конституциональная – при ней наблюдаются задержка роста костей и появление вторичных признаков у соматически здоровых девочек.
- Гипогонадотропный гипогонадизм – недостаточность синтеза гонадотропных гормонов.
- Гипогонадотропный гипергонадизм – отсутствие секреции гормонов половых желез.
Выраженность каждой патологии может отличаться, а лечение зависит от точной причины появления.
Конституциональная форма
Патология часто является врожденной и передается по наследству. Конституциональная задержка полового развития действует через врожденные или приобретенные нарушения секреции гипоталамического ЛГ релизинг-фактора. Патогенез заболевания до конца не известен. Но не исключается действие различных патологических факторов, которые приводят к поздней активации системы гипоталамус-гипофиз-яичники.
Также возможна функциональная гиперпролактинемия, что приводит к нарушению синтеза дофамина, а также к уменьшению импульсного выделения гонадотропных гормонов и соматотропина. Также отмечаются изменения в секреции катехоламинов: уменьшение секреции адреналина и норадреналина, и увеличение серотонина.
Особенностями конституциональной ЗПР является пропорциональное отставание в росте, но при этом появление вторичных половых признаков происходит согласно костному возрасту, который может опережать паспортные данные.
Для девочек с такой патологией взросление дается не легко. Организму требуется значительно больше времени на достижение возраста, заложенного генетически. Рост может задерживаться до 19 лет и дольше.
Обращение к врачу часто происходит после субъективной оценки своих данных. Родители девочки или она сама отмечают отсутствия скачка в росте характерного для этого состояния, отсутствие фенотипических измерений.
Аналогичные нарушения роста часто возможны у ближайших родственников. Но после запуска полового созревания постепенно разница между половыми признаками и костным возрастом становится незаметной.
Гипогонадотроный гипогонадизм
Задержка полового развития центрального генеза может быть связана с минимальными изменениями в мозговых центрах, а также при опухолевых и неопухолевых образованиях. Но основу патологии составляют недостаточность секреции гонадотропных гормонов из-за врожденной или приобретенной функции нарушения ЦНС. Состояние может наблюдаться в следующих случаях:
- аномалии мозговых сосудов;
- гипоплазия передней доли гипофиза;
- последствия туберкулеза, сифилиса, саркоидоза;
- пострадиационные изменения в результате облучения;
- состояние после травмы головы.
Гипогонадотропный гипогонадизм также может быть последствием тяжелых системных хронических патологий:
- тяжелые пороки сердца;
- почечная, печеночная недостаточность;
- серповидноклеточная анемия;
- талассемия;
- болезнь Гоше;
- болезнь Крона;
- муковисцидоз (и другие варианты патологий пищеварительного тракта).

Хронические инфекции, а также ВИЧ могут стать причиной поражения гипоталамуса. Повышенные физические нагрузки, неполноценное питание, нарушение пищевого поведения (анорексия или булимия), длительное лечение психотропными препаратами, глюкокортикоидами негативно может повлиять на состояние гипофизарно-яичниковой оси. Экология также сказывается на темпах развития. Установлено, что увеличение в крови свинца до 3 мкг/дл приводит к задержке развития на 3-6 месяцев.
Гипергонадотропный гипогонадизм
ЗПР яичникового генеза часто связана с дисгенезией или агенезией гонад. Также причины могут быть в хромосомных или генетических отклонениях:
- синдром Тернера;
- дисгенезия гонад при кариотипе 46 х.
Нарушение созревания может происходить на фоне метаболических расстройств, приводящих к нарушению синтеза гормонов.
В ряде случаев ЗПС является следствием аутоиммунного заболевания, при этом наблюдается проявление признаков:
- сахарного диабета;
- тиреоидита;
- синдрома атаксии телеангиэктазии.
При данной патологии может наблюдаться дефицит ферментов, участвующих в образовании гормонов яичников. У девочек на фоне гипергонадотропного гипогонадизма может развиваться устойчивая артериальная гипертензия, в крови отмечается повышенная концентрация прогестерона.
Редко патология обусловлена недостаточностью яичников, развивающейся вследствие удаления части или всего органа, применения некоторых лекарственных средств или ионизирующего облучения.
Правила диагностики
Для установления причин патологии у девочки обязательно выясняется семейный анамнез в беседе с родителями, предпочтительнее с матерью. Также оцениваются:
- течение беременности;
- наличие ее осложнений;
- течение периода новорожденности;
- этапы взросления и их соответствие нормам;
- перенесенные патологии.
Следует помнить, что диагностика начинается только с приближением периода полового созревания, когда можно с уверенностью говорить от степени зрелости и появлении необходимых признаков.
Осмотр
В плане диагностики обязательно проводят тщательный общий осмотр, во время которого фиксируют рост, вес, распределение и степень выраженности клетчатки
Необходимо обратить внимание на следы возможных операций, шрамы, которые могли быть результатом травм
Вагинальный осмотр проводится в присутствии матери или законного представителя ребенка. Для него применяют специальные детские зеркала. В некоторых случаях вагинальный осмотр заменяют ректальным, который следует проводить после очистительной клизмы.
Лабораторные исследования
Кровь на гормоны сдается натощак и в полном объеме. Необходимо определение ЛГ и ФСГ, эстрадиола и ДГЭАС. По показаниям производят исследование концентрации прогестерона, пролактина, кортизола, СТГ, ТТГ, антитела к Т4-а, к тиреоидной пероксидазе.
У девочек с костным возрастом более 11 лет проводят пробу с агонистами гонадотропинов. В более младшем возрасте, исследование не информативно. Через 5-7 дней после постановки пробы проводят анализ на эстрадиол. При функциональной ЗПР и дефектах рецепторов к гормону происходит его увеличение в крови.
Также применяют определение через каждых 20-30 минут секреции ЛГ в ночное время и суммарную секрецию с мочой. Если наблюдается его увеличение и в ночные часы, это говорит в пользу конституциональной ЗПР. Отсутствие разницы между концентрацией ночью и в течение дня говорит в пользу гипогонадотропного гипогонадизма.
Клинические рекомендации при задержке полового развития включают определение кариотипа. Это позволяет выявить Y хромосому или некоторые мутантные гены, что определяет дальнейшую тактику лечения.
Выявление аутоантител к яичникам говорит об аутоиммунной природе патологии.
Инструментальные методы диагностики
Включают выполнение УЗИ органов малого таза для определения степени развития половых органов. Также УЗИ необходимо в момент постановки функциональной пробы чтобы выяснить, как откликнулись яичники на стимуляцию гормонами.
Если задержка развития имеет конституциональную природу, то на УЗИ матки и яичники остаются в допубертатном размере, могут иметься единичные фолликулы. При остальных вариантах ЗПР матка и придатки имеют низкую степень развития, иногда даже представлены тяжами тканей.
Выполняют УЗИ молочных желез, которые находятся в состоянии покоя, характерном для допубертатного возраста.
Объемные образования головного мозга определяют с помощью МРТ. Опухоль должна иметь размер более 5 мм, чтобы ее можно было заметить во время исследования. Также может наблюдаться изменение строения сосудов, питания участков нейрогипофиза и других зон головного мозга.
Также применяют следующие методы диагностики:
- денситометрию;
- офтальмоскопию;
- рентгенографию черепа;
- проверку слуха;
- диагностику обоняния.
Эти методики имеют значение при диагностике некоторых генетических синдромов, которые не всегда можно подозревать.
Дополнительные обследования при задержке полового развития
На основании анамнеза заболевания и объективного обследования можно выставить предварительный диагноз. В дальнейшем необходимо определить базальную концентрацию тестостерона или эстрадиола, гонадотропина, а также оценить костный возраст. Для оценки функции половых желез информативно определение уровня ингибина. При постоянном гиперили гипогонадотропном гипогонадизме костный возраст может быть выше 11 лет (у девочек) и 13 лет (у мальчиков) при отсутствии признаков полового созревания; при временном дефиците это встречается нечасто. Дополнительные исследования зависят от вида задержки полового созревания – гипо или гипергонадизма.
Гипергонадотропный гипогонадизм
Гипергонадотропный гипогонадизм диагностируют при увеличении концентрации гонадотропинов; часто концентрация ФСГ значительно превышает таковую ЛГ.
Даже при нормально сформированных половых органах показано проведение кариотипирования. Для исключения тканевого мозаицизма необходимо взять образцы крови и фибробластов.
При наличии гипертензии в диагностике нарушений синтеза стероидов поможет определение профиля стероидов надпочечников в моче.
При наличии полосковидных половых желез на УЗИ органов малого таза выявляются отсутствующие или маленькие допубертатные яичники.
Если у мальчика не удается пропальпировать яички, их локализация может устанавливаться по данным УЗИ либо в паховом канале, либо во внутрибрюшной полости. Для определения функционирующей ткани гонад можно провести короткую ХГЧ-пробу. Назначение ЛГ-подобного лекарственного препарата вызывает выработку эстрогена и тестостерона, что можно выявить путем повышения их значений относительно базального уровня. Иногда для точного доказательства отсутствия ткани гонад необходимо проведение длинной пробы.
Мальчикам, у которых не пальпируются половые железы, повышена концентрация тестостерона в ответ на ХГЧ, а при УЗИ не выявлено локализации герминогенной ткани, показано проведение лапароскопии для оценки возможности проведения орхидопексии или гонадэктомии для предотвращения малигнизации.
При наличии положительного семейного анамнеза или соответствующих клинических симптомов показано определение антител к щитовидной железе, надпочечникам и яичникам.
Концентрация ингибина А у девочек и ингибина В у обоих полов — ценный маркер функции половых желез. Уровень ингибина А, вырабатываемого желтым телом, падает перед повышением уровня ФСГ при поражении яичников. Уровень ингибина В, вырабатываемого клетками гранулезы у женщин и клетками Сертоли у мужчин, падает до поражения яичников или яичек, например, после лучевой терапии; его уровень вновь повышается при нормализации функции яичек.
Гипогонадотропный гипогонадизм
Для дифференциации постоянного и временного дефицита гонадотропина показано проведение пробы с люлиберином. Результаты исследования могут быть двузначными: отсутствие повышения концентрации гонадотропина — признак центрального гипогонадизма, нечеткий ответ может наблюдаться непосредственно перед началом задержки полового созревания. Именно поэтому дифференциальная диагностика частичного центрального дефицита может представлять определенные трудности без повторных исследований перед курсами лечения и после них.
При низкорослости и признаках гипотиреоза показано проведение функциональных проб передней доли гипофиза — базальной функции щитовидной железы (Т4с), а также визуализация ЦНС при доказанном множественном дефиците.
В редких случаях низкорослость и удлиненные ноги в сравнении со спиной, что наблюдается при задержке полового созревания, может симулировать легкие формы спондилоэпифизарной дисплазии, требующей исследования скелета.